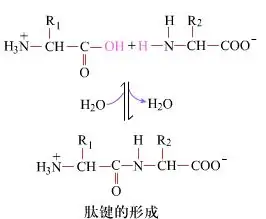
Di permukaan, pembentukan ikatan peptida, menghasilkan dipeptida, adalah proses kimia sederhana. Ini berarti bahwa kedua komponen asam amino dihubungkan oleh ikatan peptida, ikatan amida, sementara mengalami dehidrasi.
Pembentukan ikatan peptida adalah aktivasi asam amino dalam kondisi reaksi ringan. (A) Kelompok karboksil, asam amino kedua (B) Nukleofilik diaktifkan secara moiety kemudian membentuk dipeptida (A-B). "Jika komponen karboksil (a) tidak dilindungi, pembentukan ikatan peptida tidak dapat dikontrol." Produk sampingan seperti peptida linier dan siklik dapat dicampur dengan senyawa target A-B. Oleh karena itu, semua kelompok fungsional yang tidak terlibat dalam pembentukan ikatan peptida harus dilindungi dengan cara yang dapat dibalik sementara selama sintesis peptida.
Jadi, sintesis peptida - pembentukan masing -masing ikatan peptida - melibatkan tiga langkah agregasi.
Langkah pertama adalah menyiapkan beberapa asam amino yang membutuhkan perlindungan, dan struktur zwitterionik asam amino tidak ada lagi.
Langkah kedua adalah reaksi dua langkah untuk membentuk ikatan peptida, di mana gugus karboksil asam amino yang dilindungi N pertama kali diaktifkan ke perantara aktif dan kemudian ikatan peptida terbentuk. Reaksi digabungkan ini dapat terjadi sebagai reaksi satu langkah atau sebagai dua reaksi berurutan.
Langkah ketiga adalah penghapusan selektif atau penghapusan lengkap basis pelindung. Meskipun semua pemindahan hanya dapat terjadi setelah semua rantai peptida telah dirakit, pemindahan selektif dari kelompok pelindung juga diperlukan untuk melanjutkan sintesis peptida.
Karena 10 asam amino (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, SEC dan CYS) mengandung gugus fungsi rantai samping, yang membutuhkan perlindungan selektif, membuat sintesis peptida lebih rumit. Basis perlindungan sementara dan semi-permanen harus dibedakan karena persyaratan yang berbeda untuk selektivitas. Kelompok perlindungan sementara digunakan pada langkah berikutnya untuk mencerminkan perlindungan sementara asam amino atau kelompok fungsional karboksil. Kelompok pelindung semi-permanen dihilangkan tanpa mengganggu ikatan peptida yang sudah terbentuk atau rantai samping asam amino, kadang-kadang selama sintesis.
“Idealnya, aktivasi komponen karboksil dan pembentukan ikatan peptida selanjutnya (reaksi kopling) harus cepat, tanpa pembentukan rasemia atau produk sampingan, dan reaktan molar harus diterapkan untuk mencapai hasil tinggi.” Sayangnya, tidak ada metode kopling kimia yang memenuhi persyaratan ini, dan sedikit yang cocok untuk sintesis praktis.
Selama sintesis peptida, kelompok fungsional yang terlibat dalam berbagai reaksi biasanya terkait dengan pusat manual, glisin menjadi satu -satunya pengecualian, dan ada potensi risiko rotasi.
Langkah terakhir dalam siklus sintesis peptida adalah penghapusan semua kelompok pelindung. Penghapusan selektif dari kelompok pelindung penting untuk ekstensi rantai peptida selain persyaratan untuk menghilangkan perlindungan lengkap dalam sintesis dipeptida. Strategi sintetis harus direncanakan dengan cermat. Bergantung pada pilihan strategis, N dapat secara selektif menghapus kelompok pelindung α-amino atau karboksil. Istilah "strategi" mengacu pada urutan reaksi kondensasi dari asam amino individu. Secara umum, ada perbedaan antara sintesis bertahap dan kondensasi fragmen. Sintesis peptida (juga dikenal sebagai "sintesis konvensional") terjadi dalam larutan. Dalam kebanyakan kasus, pemanjangan rantai peptida secara bertahap hanya dapat disintesis dengan menggunakan rantai peptida untuk mensintesis fragmen yang lebih pendek. Untuk mensintesis peptida yang lebih lama, molekul target harus disegmentasi menjadi fragmen yang sesuai dan ditentukan bahwa mereka dapat meminimalkan tingkat diferensiasi pada terminal C. Setelah fragmen individu secara bertahap dirakit, senyawa target akan bergabung. Strategi sintesis peptida mencakup pemilihan fragmen pelindung terbaik dan paling tepat, dan strategi sintesis peptida mencakup pemilihan kombinasi yang paling tepat dari basis pelindung dan metode konjugasi fragmen terbaik.
Waktu posting: 2025-07-02